В настоящее время преобладающая часть фармацевтических препаратов поступает в Республику Казахстан из стран ближнего и дальнего зарубежья, в то время главной целью отреслевой программы развития отечественной фармацевтической промышленности является планомерное снижение зависимости от импорта лекарственных препаратов. Следовательно, изучение химического состава некоторых растений,выделение биологически активных комплексов и разработка новых лекарственных средств с заданными свойствами является важной и актуальной задачей.
Объектом наших исследований является надземная часть травы верблюжьей колючки киргизской родаAlhagiAdans( AlHAGI KIRGISORUM SCHRENK). Из этого растения получена субстанция «Алхидин», где действующим началом является полимерный проантоцианидин.Субстанция «Алхидин» (РК-ЛС-3-№004762)зарегистрирован в республике Казахстан, как новый отечественный препарат.
Субстанция «Алхидин» состоит изконденсированногодубильного вещества представляющий собой проантоцианидин на основе (+)-катехина и (-)-эпигаллокатехина с С4-С8 (С6)- формой связи, дубильного вещества гидролизуемого типа,флавоноловых моно-, дигликозидовизорамнетина,кверцетина, аминокислот, водорастворимогогетерополисахарида, витамина С, Е, каротина, макро- и микроэлементов.
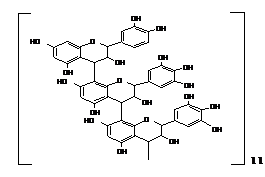
Полимерный проантоцианидин — (С45Н34О18)11 зарегистрирован в НИИ по биологическим испытаниям химических соединений за № 2946580[1-5].
Рихлокаин- синтетический анестезирующий отечественный препарат, который разработан на кафедре химии и технологии органических веществ, природных соединений и полимеров КазНУ им.аль-Фараби[6-7].
Изучение эффективности препаратовна основе Алхидина и Рихлокаина проводилось на базе Испытательного Центра РГП на ПХВ «Национальный Центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники» МЗ РК, в лаборатории фармакологических испытаний, под руководством зав.лабораторией фармакологических испытаний Шнаукшта В.С. и главного специалиста лаборатории фармакологическихиспытаний Байзаковой К.К и сотрудниками [8-11].
Материалы и методы
Исследования проводили в соответствии с утвержденным протоколом доклинического исследования №ДИП-13-24 на белых лабораторных крысах. Животные распределялись по группам случайным образом. В качестве критерия приемлемой рандомизации считали отсутствие внешних признаков заболевания и гомогенность групп по массе тела (±10 %).
Исследование фармакологической (ранозаживляющей) активности.
Изучение ранозаживляющего действия испытуемых образцов проводили на модели термического ожога кожи. В эксперименте использовали беспородных крыс массой 180 – 200 грамм, содержащихся в стандартных условиях вивария.
Модельтермического ожогавоспроизводилиу предварительно депилированных крыс под эфирным наркозом путем аппликации металлической пластинки общей площадью 113 кв.мм, нагретой до 67,0 ±0,5С°. Время экспозиции составит 5 с. Дефекты кожи оставались открытыми на протяжении всего периода наблюдения.
О динамике ожогового повреждения судили по площади раны. Темпы заживления ожога у крыс из разных групп оценивали с помощью веса периодически прорисованных на кальку конфигурации ран. Ежедневно оценивали внешний вид ран, наличие и характер отделяемого, отмечали сроки заживления. Статистическая обработка полученных результатов проводилась с применением метода наименьших квадратов.
Оценку общего состояния животных проводили на основании поведенческих реакций, аппетита, массы тела, выживаемости. Наблюдение за процессом заживления ожоговых ран проводили ежедневно, а величина ожоговых дефектов измеряли периодически на протяжении исследования. Оценку ранозаживляющего действия проводили по характеру клинического течения (наличия нагноения, времени полного отторженияструпа, времени и динамике полного срастаниякраев раны) на 2, 7, 14, 21 и 28 дни наблюдения.Последние наносили ежедневнона раневую поверхность животным остальных экспериментальных групп. Препараты наносили,начиная со второго дня после нанесения ожога до полного заживления ран.Процесс регенерации изучаличерез дискретные промежутки времени по изменению площади раневой поверхности, состоянию раны. У контрольных животных происходилоспонтанноеранозаживление.
Из животных были сформированы однородные по массе тела группы по 5 особей в каждой (таблица 1).
Таблица 1. Группы экспериментальных животных
| Номер группы | Количество животных | Препарат, путь введения и объем (доза) |
| Группа №1 | 5 | Контроль — нелеченные животные |
| Группа №2 | 5 | Алхидин 3 % |
| Группа №3 | 5 | Алхидин 5% |
| Группа №4 | 5 | Алхидин 10 % |
| Группа №5 | 5 | Алхидиновая мазь 10% |
| Группа №11 | 5 | Рихлокаин 0,5% |
| Группа №12 | 5 | Рихлокаин1 % |
| Группа №13 | 5 | Рихлокаин 1% + Алхидин 5% |
| Группа №14 | 5 | Рихлокаин 1% + Алхидин 10 % |
| Группа №18 | 5 | Aqua Dress Алхидин5 % |
| Группа №19 | 5 | Aqua Dress Алхидин10 % |
| Группа №21 | 5 | AquaDressРихлокаин1 % |
| Группа №23 | 5 | AquaDressРихлокаин1 %+ Алхидин 5 % |
| Группа №24 | 5 | AquaDressРихлокаин1 %+ Алхидин10 % |
| Группа №25 | 5 | Диклофенак гель |
При проведении экспериментов по исследованию фармакологической активности исходили из требований действующей ГФ РК первое издание, и «Руководства по экспериментальному (доклиническому) изучению новых фармакологических веществ» под ред. член-корр. РАМН, профессора Хабриева Р.У. Москва, 2005 г.
Результаты работы и их обсуждение.
Через сутки после нанесения ожога состояние и площадь раневой поверхности контрольных и опытных животных практически не отличались: ярко выраженная гиперемия, отек, элементы некроза. Со 2-го дня эксперимента было начато нанесение исследуемых образцов. Полученные результаты о влиянии гелей в различной концентрации данных средств на процесс заживления ожогового дефекта представлены в таблице 2.
Таблица 2. Динамика состояния раневой поверхности кожи животных при исследовании ранозаживляющей активности изучаемыхгелей
|
№ |
Вводимое
соединение |
Вес кальки (мг) |
||||
| исходный | 7 день | 14 день | 21 день | 28 день | ||
| 1 | контроль | 93,7±18,6 | 85,7±16,1 | 32,7±4,3 | 16,3±5,8 | 9,8±0,9 |
| 2 | Алхидин 3 % | 79,3±10,1 | 60,0±10,8 | 31,7±9,9 | 9,7±1,8 | 0,0±0,0 |
| 3 | Алхидин 5% | 69,7±14,4 | 51,7±12,3 | 23,3±3,8 | 7,7±2,2 | 0,0±0,0 |
| 4 | Алхидин 10 % | 52,7±2,7 | 24,0±1,5 | 0,0±0,0 | 0,0±0,0 | 0,0±0,0 |
| 5 | Алхидиноваямазь 10% | 60,7±7,3 | 38,0±11,1 | 29,0±7,0 | 18,7±4,6 | 0,0±0,0 |
| 11 | Рихлокаин 0,5% | 85,3±16,8 | 76,7±14,2 | 23,3±3,8 | 7,7±4,6 | 0,0±0,0 |
| 12 | Рихлокаин1 % | 97,3±22,3 | 84,0±17,8 | 16,0±1,4 | 6,3±2,0 | 0,0±0,0 |
| 13 | Рихлокаин 1% + Алхидин 5% | 121,7±10,2 | 100,0±22,2 | 51,3±5,5 | 14,0±4,4 | 0,0±0,0 |
| 14 | Рихлокаин 1% + Алхидин 10 % | 130,0±14,2 | 133,0±12,9 | 51,3±6,2 | 18,3±2,0 | 0,0±0,0 |
| 18 | Aqua Dress Алхидин5 % | 74,0±1,2 | 42,7±0,3 | 15,7±0,9 | 4,9±1,8 | 0,0±0,0 |
| 19 | Aqua Dress Алхидин10 % | 72,7±1,7 | 40,3±0,9 | 14,3±0,7 | 3,3±1,7 | 0,0±0,0 |
| 21 | AquaDressРихлокаин1 % | 77,0±2,3 | 30,3±0,9 | 14,3±0,7 | 5,3±0,9
|
0,0±0,0 |
| 23 | AquaDressРихлокаин1 %+ Алхидин 5 % | 75,3±6,7 | 41,7±0,7 | 19,0±5,1 | 6,0±1,0 | 0,0±0,0 |
| 24 | AquaDressРихло-каин1 %+ Алхидин10 % | 79,3±2,9 | 34,3±2,3 | 18,7±2,3 | 3,0±1,5 | 0,0±0,0 |
| 25 | Диклофенак гель | 96,7±40,9 | 99,3±24,0 | 50,7±14,3 | 39,3±11,1 | 12,4±2,7 |
Анализ полученных данных на 21 день эксперимента выявил наличие выраженной репаративной активности у геля Алхидин. Следует отметить связь эффективности с концентрацией исследуемого образца. Наибольшую активность проявил Алхидин в 10% концентрации применение, которого уже на 14 день сопровождалось полным заживлением термической раны.
Активность Рихлокаина повышалась с возрастанием концентрации активного соединения. Остальные исследуемые соединения в аналогичных условиях оказали менее выраженные ранозаживляющие эффекты.
Следует отметить, что процесс заживления термических ожогов проходил без гнойно-воспалительной реакции окружающих тканей. О ранозаживляющей активности также судили по срокам заживления термического ожога (таблица 3).
Таблица 3. Влияние исследуемых соединений на сроки заживления термического ожога у крыс
|
Группа наблюдения |
Сроки заживления (дни) |
Ускорение заживления раны по отношению к контрольной группе, % |
| контроль | 27,7±1,5 | 82,6 |
| Алхидин 3 % | 23,3±2,4 | 87,8 |
| Алхидин 5% | 22,0±1,7 | 89,0 |
| Алхидин 10 % | 9,0±1,0 | 100 |
| Алхидиновая мазь 10% | 27,3±1,2 | 69,2 |
| Рихлокаин 0,5% | 17,0±2,5 | 91,0 |
| Рихлокаин1 % | 14,0±5,5 | 93,5 |
| Рихлокаин 1% + Алхидин 5% | 25,3±4,8 | 88,5 |
| Рихлокаин 1% + Алхидин 10 % | 24,3±2,8 | 86,0 |
| Aqua Dress Алхидин5 % | 19,3±1,9 | 93,4 |
| Aqua Dress Алхидин10 % | 17,3±4,2 | 95,5 |
| AquaDressРихлокаин 0,25 % | 15,0±1,7 | 92,3 |
| AquaDressРихлокаин1 % | 10,3±0,9 | 93,1 |
| AquaDressРихлокаин1 %+ Алхидин 5 % | 19,3±2,2 | 92,0 |
| AquaDressРихлокаин1 %+ Алхидин10 % | 17,0±2,5 | 96,2 |
| Диклофенак гель | 32,3±2,0 | 59,4 |
У группы нелеченных животных заживление происходило в среднем в сроки 27,7±1,5 дня. Высокую скорость заживления продемонстрировали Алхидин гель 10 % и повязка AquaDressРихлокаин 2 %. Нанесение данных препаратов сопровождалось полной эпителизацией кожи в течение 9,0±1,0 и 9,0±0,6 дней. Высокую ранозаживляющую активность проявил также препарат Рихлокаин в 1% концентрации, представленного как в виде геля, так и в виде повязки.Остальные соединения продемонстрировали меньшую ранозаживляющую активность. Самые низкие показатели отмечены у препарата сравнения Диклофенак и Лимонидиновой мази. Следует отметить, что процесс заживления у подопытных животных не сопровождался гнойно-воспалительной реакцией окружающих тканей, образованием гнойно-некротических корочек.
ЗАКЛЮЧЕНИЕ
Проведено доклиническое скрининговое исследование ранозаживляющей активности биологически активных соединений Лимонидин гель, Алхидин гель, Рихлокаин гель, комбинированных гелей (Рихлокаин+Лимонидин, Рихлокаин+Алхидин), повязок (AquaDressАлхидин, AquaDressРихлокаин, AquaDressРихлокаин+Алхидин) производства ТОО «Химия и Инновация», Республика Казахстан.
Проведенное экспериментальное изучение фармакологической (репаративной) активности представленных гелей и повязок показало, что Алхидин гель 10 %-ной концентрации по показателю скорости и активности заживления обладает высокой репаративной активностью и значительно ускоряет заживление термической раны относительно первоначальной площади. Остальные соединения обладают меньшей ранозаживляющей активностью.
Списоклитературы:
- Бурашева Г.Ш., Абилов Ж.А., Рахимов К.Д. Трава верблюжья колючка киргизская. ФС РК 42-228-99
- Бурашева Г.Ш., Абилов Ж.А., Рахимов К.Д. Биологически активный комплекс – алхидин и его фармакологическая активность.- Алматы.- 2001.- 180 с.
- Бурашева Г.Ш., Абилов Ж.А., Рахимов К.Д. Субстанция «Алхидин». ВФС РК 42-389-01.
- Бурашева Г.Ш., Абилов Ж.А., Рахимов К.Д. Субстанция «Алхидин». РК-ЛС-3- № 004762.
- Предпатент №10991 РК. МПК А 61К 35/78. Противовоспалительное, ранозаживляющее, противоожоговое фармакологическое средство./ Г.Ш.Бурашева и др.Опубл.14.12.2001. бюл.№12.
- ISO 10993-5:2009. Biological evaluation of medical devices — Part 5: Tests for in vitro cytotoxicity
- ГОСТ Р ИСО 10993-5-2009. Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 5. Исследования на цитотоксичность: методы invitro.
- «Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ» Под ред.члена–корр.РАМН, проф.Р.У.Хабриева, Москва, 2005 г.
- Катцунг Б.Г. – Базисная и клиническая фармакология. Санкт-Петербург, 1998, т 2.
- Лоуренс Д.Р., Беннет П.Н., Браун М.Дж. – Клиническая фармакология. Москва, «Медицина»,2002 г.
- A Guide to the Management Hazardous Substances. — . https://www.ccohs.ca/oshanswers/chemicals/ld50.html.[schema type=»book» name=»НОВЫЕ ОТЕЧЕСТВЕННЫЕ РАНОЗАЖИВЛЯЮЩИЕ ПОВЯЗКИ И МАЗЕЙ НА ОСНОВЕ АЛХИДИНА И РИХЛОКАИНА» description=»Объектом наших исследований является надземная часть травы верблюжьей колючки киргизской родаAlhagiAdans( AlHAGI KIRGISORUM SCHRENK).Проведено доклиническое скрининговое исследование ранозаживляющей активности биологически активных соединений Лимонидин гель, Алхидин гель, Рихлокаин гель, комбинированных гелей (Рихлокаин+Лимонидин, Рихлокаин+Алхидин), повязок (AquaDressАлхидин, AquaDressРихлокаин, AquaDressРихлокаин+Алхидин) производства ТОО «Химия и Инновация», Республика Казахстан. » author=»Темирханова Гулден Ерлановна, Мун Григорий Алексеевич » publisher=»БАСАРАНОВИЧ ЕКАТЕРИНА» pubdate=»2017-03-04″ edition=»ЕВРАЗИЙСКИЙ СОЮЗ УЧЕНЫХ_27.06.2015_06(15)» ebook=»yes» ]

