Активные угли (АУ) широко используются для очистки природных и сточных вод от органических загрязнителей. При этом предполагают, что адсорбция органических компонентов протекает за счет дисперсионного взаимодействия. Однако наличие в структуре молекулы полярных функциональных групп может привести к образованию водородных или донорно-акцепторных связей с поверхностными соединениями кислорода, образованными в процессе получения активных углей.
Целью работы было исследование адсорбции анилина дроблеными активными углями, отличающимися сырьем и способом получения.
Объектами исследования выбраны активные угли марок АБГ и Пуролат-Стандарт, полученные карбонизацией и активацией в окислительной атмосфере в одну стадию, и КАД-йодный, произведенный по традиционной двустадийной технологии.
Удельная поверхность (SБЭТ), объём микро- (Vмикро) и мезопор (Vмезо) образцов АУ определялись по низкотемпературной адсорбции азота, суммарный объём пор – пикнометрическим методом по воде [2, 244], объём макропор (Vмакро) рассчитывался по разнице между суммарным объёмом пор и суммой объёмов микро- и мезопор. Общее количество титруемых кислотных и основных групп на поверхности адсорбентов оценивалось по реакции обмена с растворами NaOH (СОЕ OH˗) и HCl (СОЕ H+) соответственно. Характеристики активных углей приведены в таблице 1.
Исследование пористой структуры и состояния поверхности адсорбентов показало значительные различия изученных характеристик. Установлено, что АБГ — мезопористый сорбент с преобладающими на поверхности основными группами; у Пуролат-Стандарта отсутствуют микро- и мезопоры, а поверхностные группы преимущественно кислотного типа; КАД-йодный — микропористый уголь с приблизительно равным количеством кислотных и основных групп.
Адсорбция анилина изучалась в статических условиях в интервале концентраций 0.05 – 1.0 г/дм3, при соотношении навески адсорбента к объёму анализируемого раствора, равном 1:100. Равновесная концентрация анилина определялась по собственному поглощению растворов при 230 нм. Полученные изотермы адсорбции представлены на рисунке.
Таблица 1.
Характеристика углеродных сорбентов
|
Марка АУ |
АБГ |
Пуролат-стандарт | КАД-йодный | |
| сырьё | бурый уголь | антрацит | каменный уголь | |
| карбонизация и активация | одностадийная | одностадийная | двустадийная | |
| SБЭТ, м2/г | 412 | 311 | 657 | |
| Vмакро, см3/г | 0.73 | 0.43 | 1.06 | |
| Vмезо, см3/г | 0.24 | — | 0.09 | |
| Vмикро, см3/г | 0.02 | 0.07 | 0.29 | |
| СОЕ, ммоль/г | OH˗ | 0.15 | 0.25 | 0.40 |
| H+ | 0.92 | 0.12 | 0.56 | |
Изотермы адсорбции анилина на исследованных активных углях можно отнести к H-3 типу по классификации Гильса [3, 22], что предполагает сильное специфическое взаимодействие сорбент – сорбат и начало полислойного закрепления анилина на поверхности активных углей.
Для количественного описания изотерм адсорбции в интервале области концентраций, отвечающих образованию монослоя анилина, была использована модель Ленгмюра, которая предполагает наличие определенного числа активных центров с одним и тем же сорбционным потенциалом [1, 75; 4, 575]:
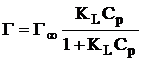 , (1)
, (1)
где Г∞ – адсорбционная емкость заполненного монослоя, моль/г, Сp – равновесная концентрация, моль/дм3; KL – константа сорбционного равновесия для монослоя, дм3/моль.
Энергия Гиббса адсорбции рассчитывалась по формуле (2) [, 85]:
![]() , (2)
, (2)
где ΔG – энергия адсорбции, Дж/моль; Т – температура, К; K – константа, полученная из уравнения Ленгмюра.
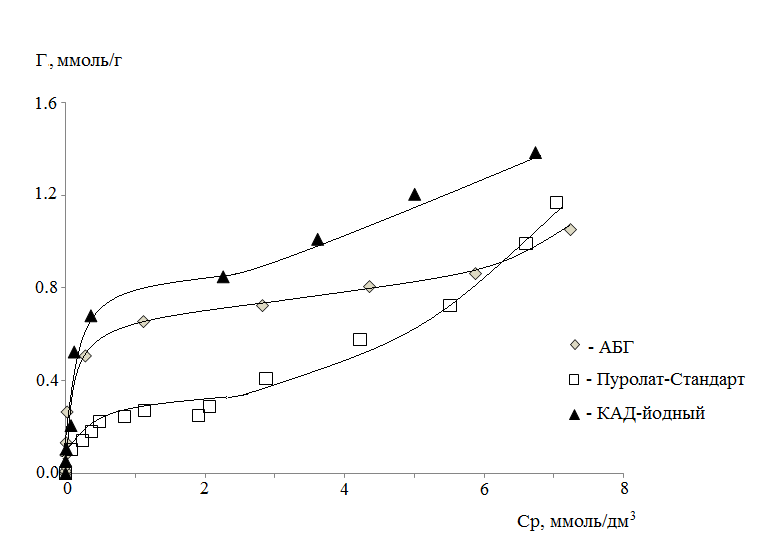
Рисунок. Изотермы адсорбции анилина из водных растворов дроблеными активными углями
Количественное описание полимолекулярной сорбции использовали модель БЭТ [4, 575]:
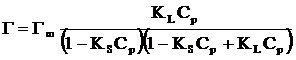 , (3)
, (3)
где KS – константа сорбционного равновесия для полимолекулярной адсорбции, дм3/моль.
Величину теплоты полимолекулярной адсорбции рассчитывали по формуле [1, 82]:
![]() . (4)
. (4)
где K – константа, полученная из уравнения БЭТ, дм3/моль.
Для определения значений констант, входящих в уравнения изотерм Ленгмюра и БЭТ, и связанных с ними термодинамических характеристик использовали линеаризованные уравнения данных моделей. Полученные значения параметров адсорбции, а также коэффициенты корреляции представлены в таблице 2.
Таблица 2.
Параметры адсорбции анилина из водных растворов АУ
| параметр | АБГ | Пуролат-Стандарт | КАД-йодный |
|
Модель Ленгмюра |
|||
| Г∞, ммоль/г | 0.73 | 0.30 | 1.02 |
| — ΔG, кДж/моль | 25.55 | 21.17 | 21.89 |
| R2 | 0.99 | 0.99 | 0.98 |
|
Модель БЭТ |
|||
| Г∞, ммоль/г | 0.53 | 0.31 | 0.77 |
| —QL, кДж/моль | 27.28 | 20.64 | 23.00 |
| —QS, кДж/моль | 9.26 | 7.37 | 10.32 |
| R2 | 1.00 | 0.99 | 1.00 |
Значения коэффициентов корреляции (R2) при линеаризации изотерм показывают, что адсорбция анилина с максимальной вероятностью описывается уравнением БЭТ.
Величины предельной емкости монослоя (Г∞), рассчитанные с использованием моделей Ленгмюра и БЭТ, сопоставимы только для АУ марки Пуролат-Стандарт, что предполагает преимущественно мономолекулярную адсорбцию анилина на этом адсорбенте. Большое различие между рассчитанными по уравнениям Ленгмюра и БЭТ значениями Г∞ (~ 35%) для АУ марок АБГ и КАД-йодный, связано, вероятно, с наличием микро- и мезопор в структуре данных адсорбентов.
Значения термодинамических характеристик взаимодействия сорбент – сорбат при образовании монослоя (ΔG и QL) подтверждают предположение о сильной специфической адсорбции анилина, которая может быть реализована за счет сильной водородной связи аминогруппы или донорно-акцепторного взаимодействия π- электронной системы молекулы анилина с поверхностными соединениями кислорода кислотного и основного типа соответственно. Наибольшее значение этих параметров характерно для АУ с наивысшим суммарным количеством кислотных и основных поверхностных групп (АБГ). Образование второго слоя при полимолекулярной адсорбции (согласно значению QS) может происходить за счет диполь — дипольного взаимодействия (например, слабой водородной связи).
Проведенные исследования показали, что в исследованной области концентраций наблюдается полимолекулярная адсорбция анилина, реализуемая за счет специфического взаимодействия сорбент – сорбат. Адсорбция анилина из разбавленных растворов наилучшим образом описывается моделью БЭТ.
Список литературы:
- Kipling J.J. Adsorption from solution of non-electrolytes. London: Academic Press, 1965. — 159 p.
- Когановский А.М., Клименко Н.А. и др. Адсорбция органических веществ из воды. Л.: Химия, 1990. — 256с.
- Парфит Г., Рочестер К. Адсорбция из растворов на поверхностях твёрдых тел: пер. с англ. М.: Мир, 1986. – 488с.
- Котова Д.Л., Фам Тхи Гам и др. Описание изотермы сорбции гидрохлорида пиридоксина на клиноптилолитовом туфе. / Сорбционные и хроматографические процессы. 2014. Т. 14. Вып. 4. С. 572 – 577.[schema type=»book» name=»ОПИСАНИЕ ИЗОТЕРМ АДСОРБЦИИ АНИЛИНА ИЗ ВОДНЫХ РАСТВОРОВ ДРОБЛЕНЫМИ АКТИВНЫМИ УГЛЯМИ» description=»Исследована адсорбция анилина из водных растворов активными углями, отличающимися сырьем, способом получения, характеристиками пористой структуры и химическим состоянием поверхности. Показано, что в исследованной области концентраций наблюдается полимолекулярная адсорбция анилина, реализуемая за счет специфического взаимодействия сорбент – сорбат. Изотермы адсорбции описаны с применением теорий Ленгмюра и БЭТ. Установлено, что сорбция анилина из разбавленных растворов наилучшим образом описывается моделью БЭТ.» author=»Беляева Оксана Владимировна, Черентаева Мария Андреевна» publisher=»БАСАРАНОВИЧ ЕКАТЕРИНА» pubdate=»2017-03-04″ edition=»ЕВРАЗИЙСКИЙ СОЮЗ УЧЕНЫХ_27.06.2015_06(15)» ebook=»yes» ]

