Введение. В связи с разработкой рядом фирм целой серии фитопрепаратов на масляной основе и их выходом на фармацевтический рынок в настоящее время возникает насущная необходимость в разработке экспрессных методов оценки антиоксидантной активности и их стандартизации. Наиболее используемой в подобных исследованиях является газометрическая методика [1-2], применение которой затруднительно из-за отсутствия выпуска специального стандартного оборудования. Поэтому, целью настоящего сообщения явилась разработка более доступной, спектрофотометрической методики оценки in vitro антиоксидантной активности растительных масел для их стандартизации.
Цепная реакция свободно-радикального окисления кумола, обычно применяемая для изучения антиоксидантных свойств веществ в газометрической методике [1-2], может быть положена в основу оценки АОА неполярных гидрофобных антиоксидантов и растительных масел спектрофотометрическим методом, если в качестве СФ-индикатора использовать ловушку радикалов N,N‘-дифенил-п-фенилендиамин (ДФФД) [3]. Одна молекула ДФФД способна быстро восстанавливать два алкильных R· или пероксильных радикала кумола RO2·, окисляясь до N,N‘-дифенил-п-бензохинондиимина (ДФБХД) с максимумом поглощения при 450 нм [4].
Материалы и методы. Реакцию окисления кумола (»1,84 моль/л) в смеси с олеиновой кислотой, взятой в концентрации 2,17 моль/л и объемном соотношении 2:1(кумол), инициировали в стеклянной нестандартной 2 мм термостатируемой кювете с помощью азо-бис(изобутиронитрила) (АИБН) концентрацией »190 ммоль/л при температуре (60,0±0,2)° C. Концентрация индикатора ДФФД, достаточная для проведения реакции, составляла 2,7 ммоль/л. В качестве раствора сравнения был взят исходный раствор ДФФД и антиоксиданта в кумоле без АИБН. О скорости окисления судили по возрастанию концентрации ДФБХД в реакционном растворе. Регистрацию кинетических кривых накопления ДФБХД осуществляли на двулучевом спектрофотометре «Specord M-40» в автоматическом режиме при 450 нм.
Результаты и их обсуждение. Схема модельной реакции окисления кумола в присутствии ДФФД без антиоксидантов представлена на рис. 1, где в качестве алкильных радикалов R· и пероксильных RO2· выступают радикалы собственно кумола. Лимитирующей стадией всего процесса окисления является наиболее медленная стадия с константой скорости образования пероксильных радикалов k1 [1].

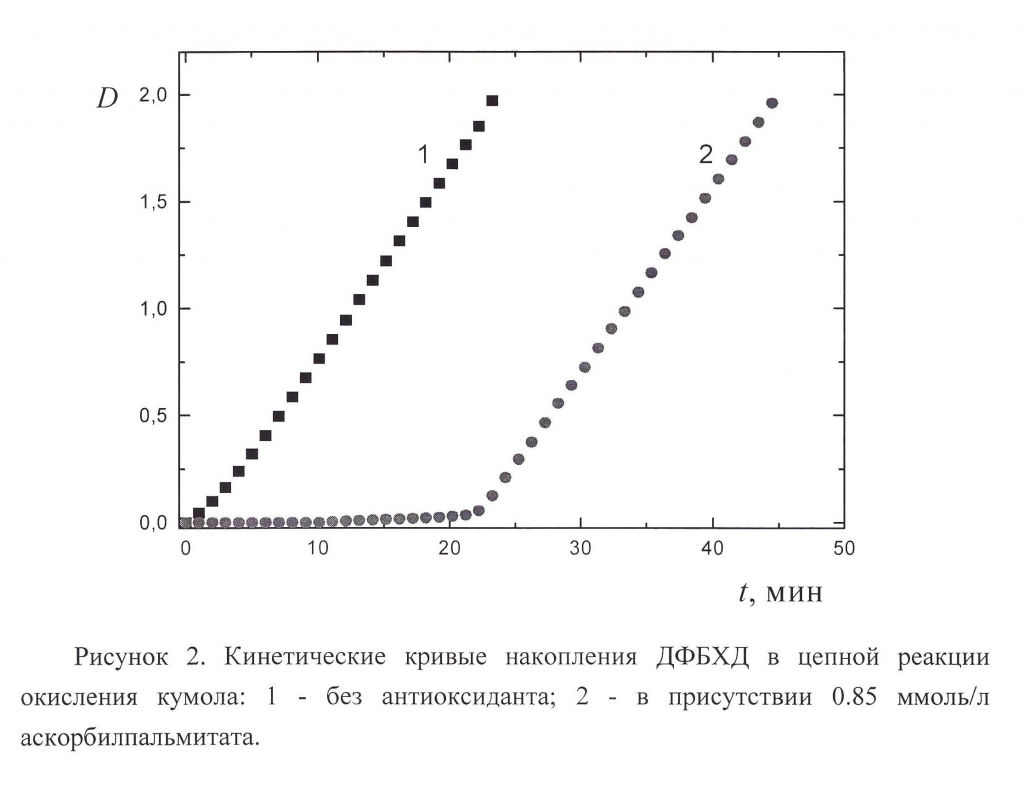
Как можно было ожидать, кривые накопления ДФБХД в реакциях окисления кумола в отсутствие антиоксидантов не имеют особенностей, характерных для ингибированного окисления [3]. В то же время, кривые накопления ДФБХД в присутствии антиоксидантов, например, аскорбилпальмитата, кверцетина и др., имеют характерные для ингибированного окисления особенности – индукционный период и/или более низкие скорости окисления (Рис. 2) [3].
Для оценки антиоксидантной активности растительных масел, в систему с кумолом вводилось масло в объемном соотношении 2 (масло):1 (кумол), при этом молярная концентрация кумола также составляла 1,84 моль/л, то есть взята избытке по отношению к концентрациям действующих антиоксидантов и азоинициатора. Оценка концентрации масла в реакционной смеси по триолеоилглицерину дает 0,69 моль/л. Достаточно большое количество введенного в реакционную смесь масла позволило сделать ощутимыми для спектрофотометрического метода концентрации действующих антиоксидантных веществ. Так, по данным ВЭЖХ в 1 кг соевого масла сумма токоферолов составляет »1400 мг (2,98 ммоль/л), а в реакционной смеси – 1,53 ммоль/л. Реакцию окисления кумола в присутствие растительных масел проводили аналогично описанному выше.
Модельную реакцию окисления кумола в присутствии антиоксидантов и растительных масел можно представить в виде схемы конкурентного ингибирования ДФФД и антиоксидантов IngH (рис.3). Отметим, что разветвлением цепи (k3) можно пренебречь, поскольку в результате использования азоинициатора обеспечивается постоянная скорость зарождения цепи, значительно превышающая скорость распада гидроперекисей ROOH.
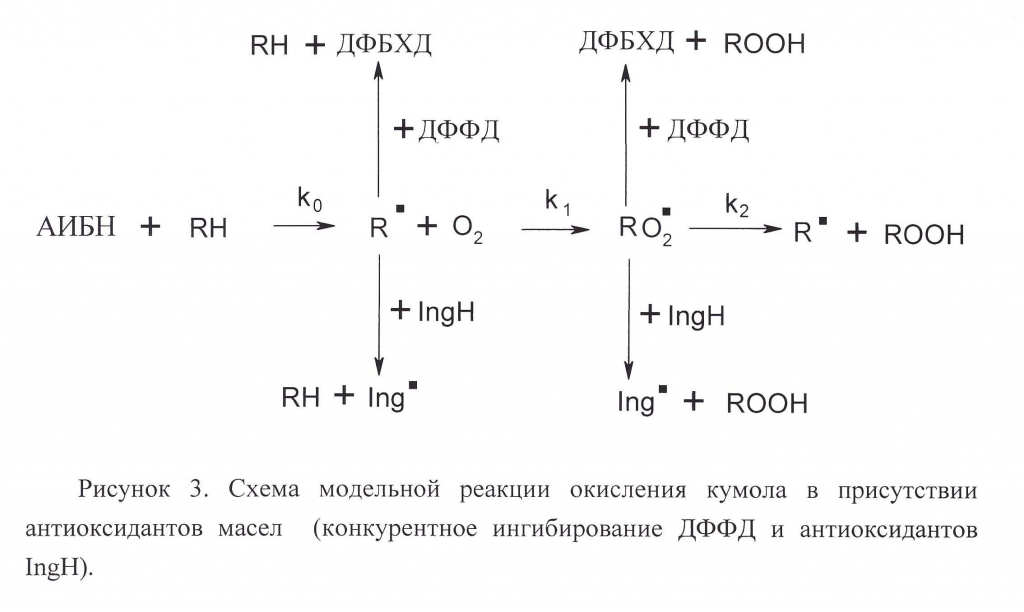
В реакционной смеси в качестве показанных на схеме (Рис. 3) алкильных R· и пероксильных RO2· радикалов могут выступать радикалы кумола, а также моно- и полиненасыщенных жирных кислот (МНЖК и ПНЖК), входящих в исследуемые растительные масла. Это приводит к параллельной множественной схеме окисления:
АИБН + R1H ® R1· + O2 ® R1O2·
АИБН + R2H ® R2· + O2 ® R2O2·
………………………
АИБН + RiH ® Ri· + O2 ® RiO2 ·,
где R1H, R2H, …, RiH – окисляемые углеводороды кумол, олеиновая, линолевая и иные ПНЖК в составе триацилглицеридов масел, а R1O2·, R2O2·,…, RiO2· — их пероксильные радикалы. Значения констант скоростей окисления k1 кумола существенно превышают соответствующие константы ki1, ki для МНЖК и ПНЖК, поскольку равновесие реакций окисления для кумола существенно сдвинуто к продуктам реакции по сравнению с равновесием для МНЖК и ПНЖК [5]. Известно также [6], что для параллельных реакций можно записать соотношение концентраций веществ
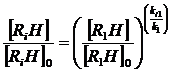 (1)
(1)
При условии k1 >> ki1 и численно равных значениях исходных концентраций кумола [R1H]0 и жирных кислот [RiH]0 из уравнения (1) можно заключить, что при протекании реакций окисления кумола на незначительную глубину [R1H] » [R1H]0, например, 5%, концентрация МНЖК и ПНЖК существенно не изменяется: [RiH] = [RiH]0. Полученная в опытах по инициированию реакций окисления кумола без ингибитора оценка глубины протекания реакции ([R1H]0 — [R1H]) / [R1H]0 составляет 0,114%. Действительно, при соотношении констант ki1/k1 = 0,05¸0,1 и концентраций [R1H] / [R1H]0 = 0,99886, содержание в реакционной смеси жирных кислот как субстратов окисления равняется исходному. Таким образом, в условиях проводимых опытов кинетика накопления ДФБХД отвечает окислению преимущественно кумола, тогда как параллельные реакции с МНЖК и ПНЖК не вносят ощутимого вклада в регистрируемую скорость окисления. Следовательно, различный жирнокислотный состав растительных масел в реакционной смеси качественно не изменяет принципиальную схему окисления (Рис. 3).
Полученные кинетические кривые окисления кумола в присутствии растительных масел, обладающих антиоксидантными свойствами, также имеют характерные для процесса ингибирования особенности – индукционный период и более низкие скорости окисления (рис. 4).
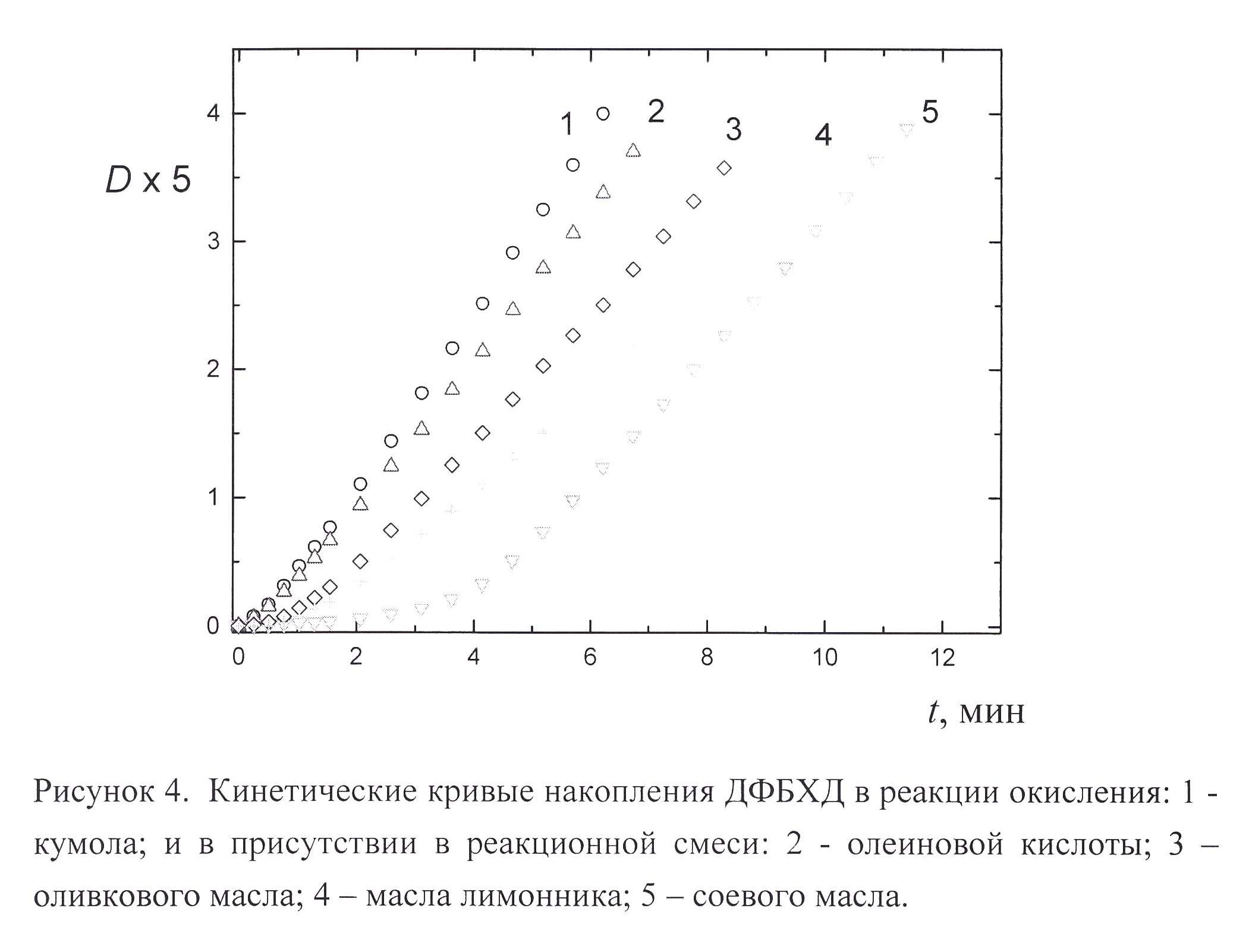
Оценку антиоксидантной активности можно проводить с учетом одновременного изменения этих параметров для различных масел, если использовать интегральный параметр – площадь под кинетической кривой в фиксированный момент времени. Отметим, что кривые накопления ДФБХД для антиоксидантов и различных масел являются существенно отличными друг от друга функциями времени вследствие различий в механизмах ингибирования для разных антиоксидантов. Использование значений площадей под кинетическими кривыми в расчетах АОА [3] позволяет, не вдаваясь в детали механизмов ингибирования и не привязываясь к форме кинетических кривых, оценить АОА для различных антиоксидантов [3] и растительных масел.
Так АОА в предлагаемой модельной системе пропорциональна разности DС(R·) концентраций алкильных и пероксильных радикалов кумола R·, образующихся в реакции (рис. 1) без ингибитора Сбланк(R·) и в реакции (рис. 3) с игибитором САО(R·), отнесенной к исходной концентрации антиоксиданта С0(АО), то есть
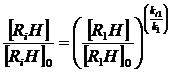 (ммоль радикалов R·/ ммоль АО) (2)
(ммоль радикалов R·/ ммоль АО) (2)
Здесь Сбланк(R·) и САО(R·) – концентрации радикалов, равные удвоенным концентрациям 2Сбланк(ДФБХД) и 2САО(ДФБХД) N,N‘-дифенил-п-бензохинондиимина соответственно [4].
Величина абсолютной антиоксидантной активности АОА, таким образом, выражает уменьшение «выхода» радикалов R· при действии антиоксиданта заданной концентрации С0(АО) по сравнению с их «выходом» в реакции без ингибитора, и тем самым характеризует эффективность действия ингибитора.
Учитывая, что величины Сбланк(R·) и САО(R·) в уравнении (2) являются существенно отличными друг от друга функциями времени Сбланк(R·) = Сбланк(t) и САО(R·) = САО(t), то можно полагать, что на промежутке времени t величина АОА определяется как
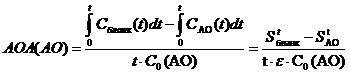 . (3)
. (3)
В числитель уравнения (3) входят значения площадей Stбланк и StАО под соответствующими кинетическими кривыми. При этом, величина (Stбланк — StАО)/e×t отвечает концентрации израсходованного за промежуток времени t антиоксиданта, а e — величина экстинции ДФБХД в реакционной смеси.
Отношение абсолютных АОА для антиоксиданта и стандартного антиоксиданта, например, кверцетина, АОА(АО)/АОА(ст), полученное из (3), дает уравнение для расчета относительной антиоксидантной активности (ОАА) на фиксированном промежутке времени t0
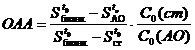 (мкмоль стандарта кверцетина/мкмоль АО). (4)
(мкмоль стандарта кверцетина/мкмоль АО). (4)
Величина ОАА показывает, во сколько раз антиоксидант с концентрацией C0(АО) эффективнее снижает «выход» радикалов на выбранном промежутке времени t0 реакции по сравнению с «выходом» радикалов при действии стандартного ингибитора концентрацией C0(ст). То есть ОАА показывает, во сколько раз 1 мкмоль антиоксиданта активнее 1 мкмоль кверцетина, и выражается в единицах мкмоль кверцетина.
Для растительных масел (РМ), обладающих антиоксидантным действием, величину ОАА определяли по формуле
 (мкмоль кверцетина / г РМ ), (5)
(мкмоль кверцетина / г РМ ), (5)
где m — масса в граммах введенного в реакционную смесь растительного масла; Vр — объем всей реакционной смеси в миллилитрах; C0(ст) — концентрация кверцетина в мкмоль/мл; SРМ, Sст, St0бланк — площади под кривыми окисления соответственно в присутствии РМ, стандартного антиоксиданта и в отсутствие РМ, но введенным в реакционную смесь таким же количеством олеиновой кислоты. Последняя в растворе с кумолом имеет близкое по величине с маслами значение экстинции.
В таблице 1 приведены значения ОАА, полученные для некоторых растительных масел на основе предлагаемого спектрофотометрического подхода. Величина ОАА показывает, во сколько раз 1 грамм растительного масла активнее 1 мкмоля кверцетина, и выражается в единицах мкмоль кверцетина / г растительного масла.
Таблица 1.
Значения ОАА некоторых растительных масел in vitro, полученные с помощью СФ-методики в модельной реакции окисления кумола
|
№№ |
Растительное масло |
ОАА , мкмоль кверцетина/ грамм РМ |
| 1. | Соевое масло | 14,37 ± 0,45 |
| 2. | Оливковое масло | 7,12 ± 0,21 |
| 3. | Масло лимонника | 10,71 ± 0,35 |
| 4. | Масло облепихи | 24,52 ± 1,20 |
| 5. | Масло расторопши | 4,65 ± 0,15 |
| 6. | w-3 ПНЖК + a-токоферол (1,15 мМ) | 9,13 ± 0,30 |
Полученная в опытах высокая активность соевого масла, очевидно, обусловлена значительно большим содержанием в нем разных свободных изомеров токоферолов по сравнению с их содержанием в оливковом масле [7]. Известно также, что ОАА масла лимонника связана содержанием в нем полифенольных соединений, главным образом, деметилированных лигнанов и флавоноидов. Последние, обусловливают также и полученное значение ОАА для масла расторопши (силибинин, силимарин). Наконец, сильный антиоксидантный эффект облепихового масла вызван, в основном, совокупным действием природных каротиноидов и токоферолов, в частности высокой константой тушения b-каротином синглетного кислорода и его антирадикальной активностью в отношении пероксильных радикалов. Для сравнения в таблице приведены значения ОАА для смеси 1,15 ммоль/л природного D-a-токоферола с w-3 ПНЖК. Вероятно, в этом случае антиоксидантный эффект объясняется синергизмом D-a-токоферола с ПНЖК, описанным в [8].
Заключение. Таким образом, несмотря на различный качественный состав антиоксидантных веществ, содержащихся в представленных растительных маслах, предлагаемая спектрофотометрическая методика позволяет оценить собственную абсолютную и относительную антиоксидантную активность in vitro как меру ингибирования модельной реакции окисления кумола. Тем самым предлагаемый подход может быть использован для стандартизации АОА различных растительных масел и комплексных фитопрепаратов на масляной основе.
Список литературы:
- Калинкина Г.И. Метод определения антиоксидантной активности растительных водно-спиртовых экстрактов. / Калинкина Г.И., Писарева С.И.// Хим.-фарм. журнал. — 1992. — №1. — С. 65 — 66.
- Ермилова Е.В. Антиокислительная активность экстрактов водяники черной. / Ермилова Е.В., Кадырова Т.В., Краснов Е.А. и др. // Хим.-фарм. журнал. — 2000. — Т. 34, № 11. — С. 28 — 30.
- Дадали Ю.В. Использование спектрофотометрического метода оценки антиоксидантной активности in vitro для стандартизации индивидуальных и комплексных фитопрепаратов. / Дадали Ю.В., Дадали В.А., Макаров В.Г. // Материалы V Международного съезда «Актуальные проблемы создания новых лекарственных препаратов природного происхождения». Санкт-Петербург-Петергоф, 2001. – С. 316 – 321.
- Noguchi N. 2,2′-azobis(4-methoxy-2,4-dimethylvaleronitrile), a new lipid-soluble azo initiator: application to oxidations of lipids and low-density lipoproteins in solution and aqueous dispersions. / Noguchi N., Yamashita H., Goton N. et. al. // Free rad. Biol. & Med. — 1998. — Vol. 24, № 2. — P. 259 — 268.
- Рогинский В.А. Исследование ингибиторов перекисного окисления липидов – акцепторов алкильных радикалов. / В сб. Исследование синтетических и природных антиоксидантов. Под ред. Бурлаковой Е.Б. М.: Наука, 1992. — С. 48 — 50.
- Эмануэль Н.М. Курс химической кинетики. / Эмануэль Н.М., Кнорре Д.Г. – М.: Высшая Школа, 1962. – С. 202.
- Н.К.Надиров. Токоферолы и их использование в медицине и сельском хозяйстве./ Н.К.Надиров. – М.: Наука, 1991. – С. 127.
- Н.М. Сторожок. Межмолекулярные взаимодействия компонентов природных липидов в процессе окисления: Автореферат дисс. … доктора хим. наук. / Н.М. Сторожок. – Москва: Ин.-т биохимической физики им. Н.М. Эмануэля РАН, 1996. – 50 c.[schema type=»book» name=»ПРИМЕНЕНИЕ СПЕКТРОФОТОМЕТРИЧЕСКОГО МЕТОДА К ОЦЕНКЕ АНТИОКСИДАНТНОЙ АКТИВНОСТИ IN VITRO РАСТИТЕЛЬНЫХ МАСЕЛ И МАСЛЯНЫХ ФИТОПРЕПАРАТОВ » description=»Нами предложена спектрофотометрическая методика оценки антиоксидантной активности растительных масел и индивидуальных гидрофобных антиоксидантов. Методика основана на ингибировании окисления изопропилбензола (кумола) антиоксидантами, содержащимися в растительных маслах. Спектрофотометрическую регистрацию процесса окисления и ингибирования окисления кумола проводили с использованием спектрофотометрического индикатора N,N’-дифенил-п-фенилендиамина, превращающегося под действием свободных алкильных и пероксильных радикалов кумола в N,N’-дифенил-п-бензохинондиимин (поглощение при 450 нм). Инициация свободных радикалов кумола осуществлялась в ходе термического разложения на радикалы инициатора азо-бис-изобутиронитрила (АИБН). Предложенный метод может быть использован для исследования и оценки антиоксидантной активности in vitro различных растительных масел и масляных фитопрепаратов. » author=»Дадали Юрий Владимирович, Дадали Владимир Абдулаевич» publisher=»БАСАРАНОВИЧ ЕКАТЕРИНА» pubdate=»2017-03-04″ edition=»ЕВРАЗИЙСКИЙ СОЮЗ УЧЕНЫХ_27.06.2015_06(15)» ebook=»yes» ]

