Экспериментальное моделирование ацетатной язвы является максимально близким аналогом клинического варианта язвенной болезни желудка и двенадцатиперстной кишки так как может подвергаться обсеменению Helicobacter pylori и хронизации процесса [4, с. 112]. При этом развитие язвенного дефекта любой этиологии является зоной инфильтративно-деструктивного воспаления тканей ЖКТ [3, с. 29-30] и сопровождается активацией стрессовых механизмов, которые в стадию тревоги и истощения стресс-реакции усиливают дисбаланс между факторами агрессии и механизмами защиты [5, с. 18-20]. При этом индивидуумы с различной устойчивостью к стрессу имеют разные механизмы реализации стресс-реакции на действие чрезмерных по силе или характеру действия повреждающих агентов [2, c. 63-64; 6, с. 55-56].
Цель. Определить роль стрессовых механизмов в стадию резистентности в формировании ацетатной язвы желудка у стрессустойчивых и стресснеустойчивых крыс.
Метод. В ходе исследования было выполнено 6 серий экспериментов на 42 белых крысах линии Вистар обоего пола под нембуталовым наркозом (40 мг/кг), предварительно разделенных на группу стрессустойчивых и стресснеустойчивых методом открытого поля. В первой и второй контрольных сериях у крыс с разной устойчивостью к стрессу выполняли все манипуляции, что и в экспериментальной серии, но без моделирования язвы. В третьей и четвертой сериях моделировалась ацетатная язва в антральной зоне на малой кривизне желудка по методу Окабэ С. [7, р. 1323], при этом крысы пятой и шестой серий подвергались острому 24-часовому иммобилизационному стрессированию через трое суток с момента моделирования ацетатной язвы. Всех животных выводили из эксперимента через 7 суток от его начала. Кровь забирали из подключичной (Vs) и портальной (Vp) вены, лимфу – из общего кишечного лимфатического протока (ОКЛП). Мочу собирали в течение суток в исходном состоянии и через 7 сут с момента моделирования контрольной серии, ацетатной язвы, ацетатной язвы на фоне стрессирования. Для исследования забирали ткани желудка с язвенным дефектом. Материал фиксировали в 10% растворе формалина в течение 2-х суток, после чего вырезали кусочки для гистологического исследования, которые заливали в парафин по стандартной методике. Гистологические срезы толщиной 5-7 мкм окрашивали гематоксилином и эозином, после чего оценивали тканевой и клеточный состав в зоне язвенных дефектов.
Для оценки функциональной активности тканей ЖКТ определяли уровень важнейшего внутриклеточного мессенджера кальция и его антагониста магния в разных биологических средах. Содержание Mg2+ в плазме крови, суточном объеме мочи и кишечной лимфе определяли реактивами набора фирмы «Лахема». Концентрацию Mg2+ в эритроцитарной массе определялся по Камышникову В. С. [1, с. 570]. Содержание Са2+ плазме крови и лимфе производили с помощью наборов фирмы «Ольвекс диагностикум» (Россия), в суточном объеме мочи – по Альгаузену А.Я.
Для статистической обработки результатов исследования при нормальном распределении использовали критерий Стьюдента (M±m).
Результат: Через 7 сут с момента моделировании ацетатной язвы у стрессустойчивых крыс площадь изъявления составляла 38,72±4,09 мм2 (рис. 1А). При микроскопии тканей края язвенного дефекта желудка был выявлен язвенный дефект, доходящий до середины мышечной оболочки, в дне которого определялись бесструктурные некротические массы, инфильтрированные обломками нейтрофилов, в более глубоких слоях – скопления нейтрофилов, лимфоцитов, и их обломков с единичными эозинофилами, в глубоких участках преобладали фибробласты. Завершение формирования язвы сопровождалось уменьшением содержания Mg2+ в эритроцитарной массе крови из Vs и Vp на 30,1% (Р<0,001) и 21,9% (Р<0,05) соответственно. Потеря Mg2+ с мочой уменьшалась на 61,5% (Р<0,001). Содержание Са2+ в кишечной лимфе увеличивалось на 33,3% (Р<0,05) на фоне снижения его потерь с мочой на 26,5% (Р<0,05), (табл.1).

Рисунок 1. Экспериментальная язва желудка на 7-е сутки у стрессустойчивых крыс: А — ацетатная язва; Б — ацетатная язва, формирующаяся на фоне острого стресса (окрашивание гематоксилин-эозином, окуляр 10, объектив 10).
У стрессустойчивых крыс со сформировавшейся под влиянием острого стресса ацетатной язвой площадь дефекта оставалась практически такой же (39,0±2,33 мм2), (рис. 1Б). Морфологические исследования выявили обширный глубокий (до середины мышечной оболочки) язвенный дефект, поверхностно в зоне язвы – бесструктурные некротические массы, инфильтрированные нейтрофилами и их обломками, глубже – молодая незрелая грануляционная ткань (капилляры, среди клеточных элементов преобладают фибробласты и лимфоциты).
Сравнительное исследование уровня Mg2+ в биологических средах у стрессустойчивых крыс со сформировавшейся ацетатной язвой под влиянием острого стресса по отношению к животным c ацетатной язвой выявило значительное его повышение в эритроцитах крови из Vs на 57,3 % (Р<0,001). Магнийурез увеличивался на 18,5% (Р<0,001). Также было выявлено в лимфе из ОКЛП повышение уровня Са2+ на 30,7% (Р<0,001) на фоне его снижения на 39,8% (Р<0,01) в суточном объеме мочи (табл.1).
Таблица 1
Площадь язвенного дефекта, уровень магния и кальция в биологических средах у стрессустойчивых крыс при экспериментальных язвах желудка
| Показатель | Контроль | Ацетатная язва | Ацетатная язва +острый стресс |
| Площадь язвы | — | 38,72±4,09 | 39,0±2,33 |
| Mg2+ в плазме крови из Vs, ммоль/л | 0,93±0,019 | 0,91±0,006 | 0,94±0,012 |
| Mg2+ в эритроцитарной массе крови из Vs, ммоль/л | 1,75±0,094 | 1,21±0,012*** | 1,90±0,143*** |
| Mg2+ в плазме крови из Vр, ммоль/л | 0,92±0,024 | 0,89±0,031 | 0,87±0,029 |
| Mg2+ в эритроцитарной массе крови из Vр, ммоль/л | 1,85±0,034 | 1,45±0,14* | 1,54±0,035 |
| Mg2+ в лимфе из ОКЛП, ммоль/л | 0,95±0,011 | 0,98±0,005 | 0,86±0,065 |
| Mg2+ в суточной моче, мкмоль/л | 18,59±0,416 | 7,15±0,19*** | 8,47±0,127*** |
| Са2+ в плазме крови из Vs, ммоль/л | 1,62±0,064 | 1,54±0,071 | 1,53±0,071 |
| Са2+ в плазме крови из Vр, ммоль/л | 1,59±0,115
|
1,69±0,079
|
1,55±0,087 |
| Са2+ в лимфе из ОКЛП, ммоль/л | 0,56±0,032 | 0,75±0,029* | 0,98±0,035*** |
| Са2+ в суточной моче, мкмоль/л | 44,09±3,40 | 32,40±2,10* | 19,50±2,40** |
Примечание: по отношению к предыдущему значению: * — Р<0,05; ** — Р<0,01; *** — Р<0,001.
У стресснеустойчивых крыс площадь язвенного дефекта при моделировании ацетатной язвы составила 68,7±9,44 мм2 (рис. 2А). При морфологическом исследовании тканей желудка был выявлен язвенный дефект, доходящий до середины мышечной оболочки; поверхностно располагались бесструктурные некротические массы инфильтрированные нейтрофилами и их обломками, далее (глубже) – лимфоциты, фибробласты, умеренное количество нейтрофилов и эозинофилов. Формирование язвы приводило к уменьшению содержания Mg2+ в эритроцитарной массе крови из Vs на 31,1% (Р<0,05). Содержание Са2+ в плазме крови из подключичной портальной вен уменьшалось на 28,6% (Р<0,001) 25% (Р<0,01) соответственно (табл. 2).
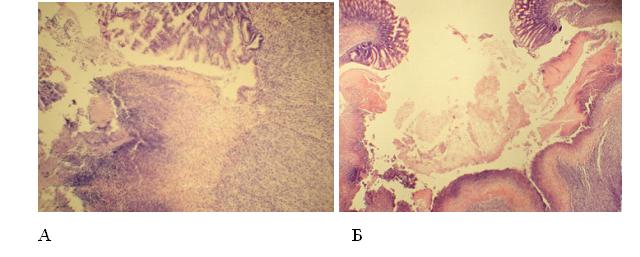
Рисунок 2. Экспериментальная язва желудка на 7-е сутки у стресснеустойчивых крыс: А — ацетатная язва; Б — ацетатная язва, формирующаяся на фоне острого стресса (окрашивание гематоксилин-эозином, окуляр 10, объектив 10).
При воздействии острого стресса на стресснеустойчивых животных со сформировавшейся ацетатной язвой площадь дефекта составила 75,7±13,94 мм2 (рис. 2Б). При этом микроскопически также был выявлен обширный язвенный дефект с некрозом, фибрином, выраженной инфильтрацией нейтрофилами и их обломками, глубже в препарате – молодая незрелая грануляционная ткань.
Сравнительное исследование содержания Mg2+ в биологических средах у стресснеустойчивых крыс показало, что острое стрессирование животных с сформировавшейся ацетатной язвой приводит к выраженному увеличению его концентрации в эритроцитах крови из Vs и Vp на 42,5 % (Р<0,05) и 24,8 % (Р<0,05) соответственно по отношению к животным с ацетатной язвой. При этом потеря Mg2+ с мочой несколько увеличивалась (Р>0,1). Концентрация Ca2+ снижалась на 30,1% (P<0,05) в суточном объеме мочи, в плазме крови из Vs и Vp и лимфе из ОКЛП оставалась неизменной (табл.2).
Таблица 2
Площадь язвенного дефекта, уровень магния и кальция в биологических средах у стресснеустойчивых крыс при экспериментальных язвах желудка
| Показатель | Контроль | Ацетатная язва | Ацетатная язва +острый стресс |
| Площадь язвы | — | 68,7±9,44 | 75,7±13,94 |
| Mg2+ в плазме крови из Vs, ммоль/л | 0,88±0,012 | 0,90±0,019 | 0,90±0,020 |
| Mg2+ в эритроцитарной массе крови из Vs, ммоль/л | 2,15±0,184 | 1,48±0,175# | 2,11±0,168# |
| Mg2+ в плазме крови из Vр, ммоль/л | 0,87±0,010 | 0,84±0,015 | 0,88±0,020 |
| Mg2+ в эритроцитарной массе крови из Vр, ммоль/л | 2,02±0,139 | 1,91±0,199 | 2,39±0,131# |
| Mg2+ в лимфе из ОКЛП, ммоль/л | 0,96±0,007 | 0,96±0,016 | 0,96±0,019 |
| Mg2+ в суточной моче, мкмоль/л | 12,81±0,527 | 15,11±2,522 | 18,24±1,93 |
| Са2+ в плазме крови из Vs, ммоль/л | 2,08±0,086 | 1,46±0,084### | 1,46±0,095 |
| Са2+ в плазме крови из Vр, ммоль/л | 1,96±0,055 | 1,53±0,088## | 1,50±0,085 |
| Са2+ в лимфе из ОКЛП, ммоль/л | 0,74±0,040 | 0,85±0,034 | 0,83±0,120 |
| Са2+ в суточной моче, мкмоль/л | 17,71±1,41 | 18,59±1,03 | 13,00±2,00# |
Примечание: по отношению к предыдущему значению: #- Р<0,05; ## — Р<0,01; ### — Р<0,001.
Анализ полученных результатов показал, что завершение формирования ацетатной язвы через 3 суток c момента ее моделирования сопровождалось снижением содержания внутриклеточного магния в эритроцитарной массе крови как у стрессустойчивых, так и стресснеустойчивых крыс. Одновременно у стрессустойчивых животных происходило уменьшение потерь c мочой магния и кальция. Через 3 суток после острого стрессирования крыс c ацетатной язвой в стадию резистентности стресс-реакции у стрессустойчивых и неустойчивых животных увеличивалось содержание магния в эритроцитарной массе крови на фоне некоторого снижения его в лимфе из общего кишечного лимфатического протока. При этом еще больше уменьшались потери c мочой ионов кальция и усиливался его перенос с кишечной лимфой у стрессустойчивых крыс. Увеличение концентрации кальция в интестинальной лимфе вероятно отражает процессы перераспределения ею макроэлементов между депо и поврежденными тканями. Накопление магния во внутриклеточном секторе является оптимизирующим условием для усиления пролиферации, т.к. интенсификация процессов пролиферации сопровождается формированием ионных каналов, по которым в клетку поступают двухвалентные катионы, и, в первую очередь, ионы магния и кальция, активизирующие в цитозоле энергетические процессы, Ca2+-зависимые протеинкиназы, синтез белков и другие молекулы. Как следует из полученных данных, стрессустойчивые животные характеризуются более оптимизированной и содружественной реакцией мобилизации и перераспределения как магния, так и кальция. У стрессустойчивых крыс накопление магния в эритроцитарной массе крови сопровождается резким снижением его потерь c мочой, в то время как у стресснеустойчивых животных на уровень его потерь с мочой стрессовые механизмы практически не влияют. Уровень магния остается стабильно высоким и регулируется только содержание кальция в обеих подгруппах животных с разной устойчивостью к стрессу.
Вывод. После острого стрессирования крыс c ацетатной язвой, сформировавшейся на фоне разной устойчивости к стрессу, отмечалось повышенное содержание внутриэритроцитарного магния на фоне его стабильно высоких потерь c мочой у стресснеустойчивых животных и значительного снижения – у стрессустойчивых. В то время как уровень кальция в суточном объеме мочи снижался в обеих подгруппах.
Список литературы:
- Камышников В.С. Справочник по клинико-биохимическим исследованиям и лабораторной диагностике. М.: МЕДпресс-информ, 2004. – 920 с.
- Поветкина В.Н., Рогова Л.Н. Удельное число клеток и интенсивность экспрессии эндотелиальной нитроксидсинтазы в тканях желудка в зоне изъязвления и уровень внутриэритроцитарного магния у стрессустойчивых и стресснеустойчивых крыс // Вестник Волгоградского государственного медицинского университета. Изд-во ВолгГМУ. № 1(45), январь-март 2013. – С. 61-64.
- Рогова Л. Н., Григорьева Н. В., Ермилов В. В., Поветкина В. Н. Концентрация магния и кальция в биологических средах и репарация тканей ЖКТ у стрессустойчивых и стресснеустойчивых крыс с экспериментальными язвами желудка до и после применения магнийсодержащей лекарственной композиции // Вестник Волгоградского государственного медицинского университета. Изд-во ВолгГМУ. № 2(46), апрель-июнь 2013. – С. 28-31.
- Рогова Л.Н., Поветкина В.Н., Григорьева Н.В., Ермилов В.В., Шестернина Н.В. Влияние стресса на формирование экспериментальной ацетатной язвы у стрессустойчивых и стресснеустойчивых крыс // Вестник Волгоградского государственного медицинского университета. Изд-во ВолгГМУ. № 4(52), октябрь-декабрь 2014. – С. 112-115.
- Порядин Г.В. Стресс и патология.- М.:РГМУ, 2009. – 23 с.
- Пшенникова М. Г. Врождённая эффективность стресс-лимитирующих систем как фактор устойчивости к стрессорным повреждениям // Успехи физиологических наук. 2003. Т. 34, №3. – С. 55-67.
- Okabe Susumu and Amagaseи An Overview of Acetic Acid Ulcer Models – The History and State of the Art Peptic Ulcer Research // Biol. Pharm. Bull. Japan, 2005. 28(8). 1321-1341.[schema type=»book» name=»РОЛЬ СТРЕССОВЫХ МЕХАНИЗМОВ В СТАДИЮ РЕЗИСТЕНТНОСТИ В ПАТОГЕНЕЗЕ ЭКСПЕРИМЕНТАЛЬНЫХ ИЗЪЯЗВЛЕНИЙ ТКАНЕЙ ЖЕЛУДКА У СТРЕССУСТОЙЧИВЫХ И СТРЕССНЕУСТОЙЧИВЫХ КРЫС» description=»Целью исследование было определение роли стрессовых механизмов в стадию резистентности в формировании ацетатной язвы желудка у стрессустойчивых и стресснеустойчивых крыс путем измерения уровня магния в эритроцитарной массе и плазме крови из разных регионов, кишечной лимфе и суточном объеме мочи, а также содержания кальция в тех же биологических жидкостях. Результаты исследования позволяют сделать вывод, что острое стрессирование стрессустойчивых и стресснеустойчивых крыс c ацетатной язвой сопровождалось повышением содержания внутриэритроцитарного магния на фоне его стабильно высоких потерь c мочой у стресснеустойчивых животных и значительного снижения – у стрессустойчивых. В то время как уровень кальция в суточном объеме мочи снижался в обеих подгруппах.» author=»Рогова Людмила Николаевна, Поветкина Виктория Николаевна, Шестернина Наталия Владимировна» publisher=»БАСАРАНОВИЧ ЕКАТЕРИНА» pubdate=»2017-03-07″ edition=»ЕВРАЗИЙСКИЙ СОЮЗ УЧЕНЫХ_27.06.2015_06(15)» ebook=»yes» ]

